葵花壳红色素提取方法
目前,食用色素主要为合成色素和从无毒无害的天然产物中提取的天然色素。合成色素虽然具有成本低、着色性好的优点,但合成色素除了改善食品的外观外,色素本身并无营养价值,且过多食用某些合成色素会严重影响人体健康[1],如在人体代谢过程中产生有害物质,以及在合成过程中还可能被砷、铅等重金属污染等缺陷。天然色素的使用安全无毒,稳定性能良好,色调自然,颜色逼真且具有相当的营养和医疗保健作用而倍受人们推崇,因此寻找和开发更多种类的天然色素已成为食用色素发展的总趋势[2-3],如红色素主要为花色素苷类,属于类黄酮化合物,具有抑制血小板凝固、预防血栓、抗癌等作用[4-6]。
油葵(oil sunflower)即油用向日葵,是我国四大油料作物之一。我国向日葵产区主要分布在西南、北方的一些地区,年产量达125万吨,而葵花籽壳是其主要副产品,作为食用油脂工业的下脚料,大部分作为燃料烧掉。而葵花籽壳中红色素含量较高,是一种较为理想的天然色素资源,因此从葵花壳中提取天然红色素既有利于农产品的深加工又有益于废弃物的回收利用。目前,对葵花壳红色素的研究有王鹏等[7]对葵花壳红色素的纯化研究,但未见对葵花壳红色素的提取条件的优化、纯化以及稳定性实验进行系统而全面的报道。本实验主要通过超声法辅助溶剂优化葵花壳红色素的提取条件;并利用乙醚沉淀法研究葵花壳红色素的纯化条件;研究光照、温度、pH值、氧化剂、还原剂以及食品添加剂对红色素稳定性影响以获得葵花壳红色素的适用范围。
1·材料与方法
1.1材料与试剂
新葵8号(产于新疆)。95%乙醇、盐酸、甲醇、丙酮、乙醚等均为分析纯。
1.2仪器与设备
TU-190双光束紫外-可见分光光度计北京普析通用仪器有限责任公司;FAZO04B电子天平上海精密科学仪器有限公司;R124旋转浓缩蒸发仪瑞士Buchi公司;MR300电磁搅拌器德国Heidolph公司;PHS-3CT酸度计上海大普仪器有限公司;L-550台式低速离心机湖南湘仪实验仪器开发有限公司;DZKV4电子恒温水浴锅北京中兴伟业仪器有限公司;KQ5200B数控超声波清洗器昆山市超声仪器有限公司;BCD243双开门冰箱广东科龙电器股份有限公司;HN101-1A电热恒温鼓风干燥箱南通沪南科学仪器有限公司。
1.3方法
1.3.1提取剂的选择
葵花壳红色素为水溶性色素,根据相似相溶原理,对红色素的提取可采用溶剂提取法。称取1g葵花壳各加入20mL蒸馏水、30%、50%、75%、80%、95%乙醇、5mL浓盐酸-50%乙醇溶液(95mL)、丙酮、乙醚、石油醚等[8-10],在50℃水浴中提取2h,过滤,并将滤液定容到100mL,以相应的溶剂作参比,在紫外分光光度计扫描后的最大吸收波长530nm测其OD值。
1.3.2超声波辅助提取葵花壳红色素正交试验
利用超声波辅助1.3.1节选择的提取剂进行优化试验,因素水平见表1、2。将提取的滤液吸取2mL入100 mL容量瓶中,并将其定容,用紫外分光光度计于53 0n m测定O D值,以确定最佳试验条件,最后,利用以上确定的优化条件进行扩大试验,并计算葵花壳红色素的粗提率。
1.4纯化试验设计
1.4.1单因素试验
1.4.1.1加入乙醚倍数的影响
称取6份红色素粗品,每份10.0g,分别用质量分数0.1%盐酸与纯甲醇的混合溶液(两溶液体积比为1:1),溶解色素粗品,抽滤;6份滤液中分别加入乙醚(加入乙醚的倍数分别为色素溶液体积的1、2、3、4、5、6倍),充分振荡后,静置于5℃冰箱中,色素以沉淀析出;重复以上相应操作直到色素以粉末状沉淀析出,得较纯色素,最后将色素沉淀置于60℃恒温鼓风干燥,得固体粉末色素,并分别将6份固体色素称量,记录。
1.4.1.2放置温度的影响
称取5份红色素粗品,余下步骤除滤液中加入乙醚倍数为上述1.4.1.1节中试验最终确定倍数;静置于冰箱中的温度分别为1、2、3、4、5℃,其余同1.4.1.1节。
1.4.2扩大试验 称取葵花壳红色素粗品20.0g,用质量分数0.1%的盐酸与纯甲醇的混合溶液(两溶液体积比为1:1),溶解色素粗品,抽滤;滤液中加入1.4.1.1节所得的加入乙醚的最佳倍数,充分振荡后,静置于冰箱中(温度为1.4.1.2试验所得的最佳温度),色素以沉淀析出;重复以上相应操作直到色素以粉末状沉淀析出,得较纯的色素,最后将色素沉淀置于60℃恒温鼓风干燥,得固体色素。

1.5稳定性实验设计
1.5.1温度对葵花壳红色素稳定性的影响
配制质量分数0.1%、pH1.0的色素溶液,以室温25℃作对照,在不同温度(25、40、60、80、100℃)恒温4.0h,每隔1.0h取1次样,冷却后分别在530nm测其OD值[11]。
1.5.2光照对葵花壳红色素稳定性的影响
配制质量分数0.1%的色素溶液,分别在室内阴暗处、室内自然光、室外自然光放置,每隔1h在530nm测其OD值,并比较OD值以确定红色素在光照下的稳定性[9,12]。
1.5.3 pH值对葵花壳红色素稳定性的影响
采用柠檬酸-磷酸二氢钾-硼酸作为稳定性试验的缓冲液,分别量取1.0mL质量分数0.1%色素溶液与9.0mL缓冲液(pH1.0~14.0)配成pH值为1.0~11.0的溶液后[13],530nm测其OD值并观察颜色变化。
1.5.4金属离子对葵花壳红色素稳定性的影响
分别将无水CaCl2、Na2SO4、无水AlCl3、CuSO4·5H2O、MgSO4配制成0.025、0.05、0.1、0.2mol/L 4个梯度浓度,分别取2mL不同浓度的Ca2+、Na+、Al3+、Cu2+、Mg2+溶液,并分别将其加入到8mL质量分数0.1%葵花壳红色素溶液中,其中,对照液为8mL质量分数0.1%葵花壳红色素溶液加2mL蒸馏水。最后,在室温阴暗处放置,每隔1h取1次样,测定其OD值,同时观察颜色变化[14]。
1.5.5氧化剂、还原剂对葵花壳红色素稳定性的影响配制H2O2、NaHSO3(质量分数梯度为0.00%、0.10%、0.30%、0.60%、0.90%、1.2%[15])溶液,分别吸取不同质量分数的氧化剂、还原剂2mL,加入8mL 0.1%葵花壳色素溶液,放置1h后,测定其OD值,同时观察颜色变化。空白组为2mL的蒸馏水加8mL 0.1%葵花壳色素溶液。
1.5.6食品添加剂对葵花壳红色素稳定性的影响
分别配制质量分数5%NaCl、10%蔗糖、20%葡萄糖溶液,吸取2mL,加入8mL的葵花壳红色素溶液(质量分数0.1%),放置1h后,测定其OD值,同时观察颜色变化。空白组是用2mL的蒸馏水来代替添加剂溶液,并将pH值调为1.0[16]。
2·结果与分析
2.1提取试验分析
2.1.1提取剂的选择
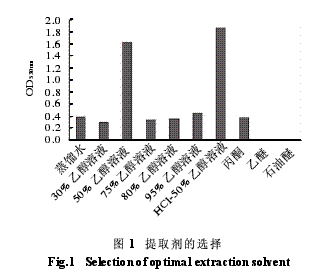
由图1分析表明:5mL浓盐酸-50%乙醇溶液(95mL)的OD值最大且颜色最深(紫红色),50%乙醇溶液次之,选择提取剂为50%盐酸-乙醇,由于色素在pH1~2较稳定,故本试验所用提取剂为pH1~2、50%酸性乙醇溶液。
2.1.2提取条件的优化
根据预试验结果,本试验设计3因素4水平的正交试验,试验设计和结果见表1。

从表1中直观分析得最优组合为1 6号处理,即A 4B 4C 1,指标为料液比1:1 6、温度5 5℃、提取时间25min。根据正交试验极差分析法[17]分析R值可知因素的主次顺序为A>C>B;通过方差分析得因素A的F=2.755>F0.10(3,15)=2.490,故A因素具有显著性;料液比、超声时间F值,但均低于F临界=2.490,均不显著。根据方差分析结果以及考虑实际成本,选取温度55℃、料液比1:16、超声时间10min为最优条件,即最优组合为A4B1C1。对所得最优组合进行验证实验,测得OD530nm为0.711,说明此组合为葵花壳红色素提取试验最优条件。
2.1.3扩大试验结果
称取10.0g葵花壳,在料液比1:16、超声温度55℃、超声时间10min条件下,对葵花壳进行色素的提取,得0.82g紫红色的色素粗品,则色素粗品的得率为8.2%。
2.2葵花壳红色素稳定性
2.2.1温度、光照对葵花壳红色素稳定性的影响

从图2可以看出:在同一pH值和时间条件下,当温度<80℃,OD530nm变化较小,颜色为深红紫色;而温度≥80℃时OD530nm变化较大,颜色由深红紫色变为红紫色最后变为淡红色。因此可以得出:温度<8 0℃时,葵花壳红色素的稳定性较好,即在温度<8 0℃条件下葵花壳红色素的耐热性较好。
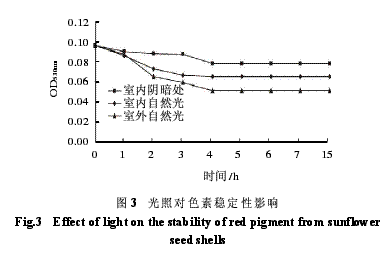
由图3可以得出:在一定试验环境下条件下,光照时间越长,OD值越小,颜色越淡,也就是说葵花壳红色素的耐光性较差。因此,葵花壳红色素应避光储藏。
2.2.2 pH值对葵花壳红色素的影响
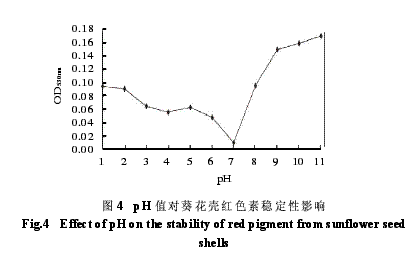
由图4可得出:当pH值在1.0~2.0的范围内时,葵花壳红色素的颜色正常,OD530nm值变化不大;当pH3.0~14.0时OD530nm值变化较大且pH值在3.0~6.0范围内时,颜色变为淡紫色,当pH值在7.0时,变为无色,pH值在8.0~11.0范围内时,变为黄绿色。故pH值在1~2范围内,葵花壳红色素的稳定性最好。
2.2.3金属离子对葵花壳红色素稳定性的影响
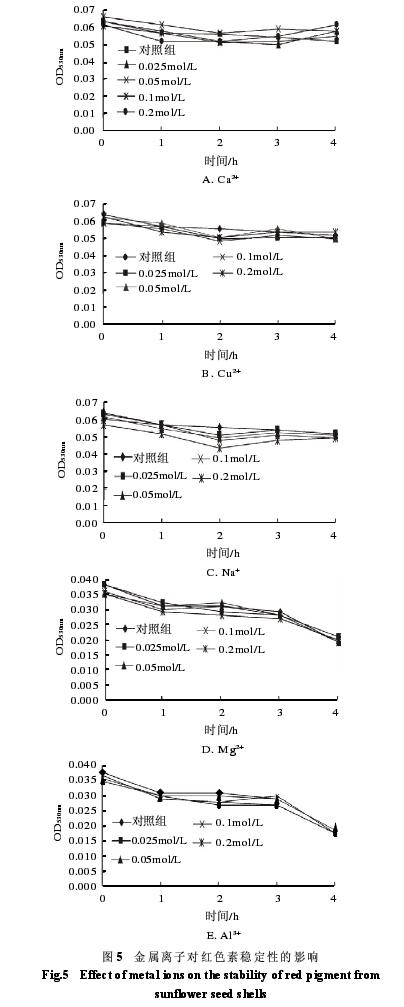
以图5为基础,分别将不同浓度下的同一金属离子的OD530nm值与之相对应的对照组的OD530nm值相比,并参照以上各图可知:随着加入金属离子Ca 2+、Na+、Al3+、Cu 2+、M g 2+浓度的增加,加入金属离子前后的OD530nm值变化不大,且颜色变化不大,说明金属离子对葵花壳红色素稳定性的影响不大。
2.2.4氧化剂、还原剂对葵花壳红色素稳定性的影响
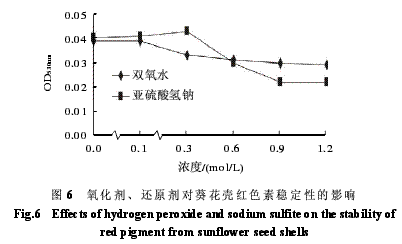
由图6可知,随着氧化剂和还原剂浓度的增加,葵花壳红色素的颜色始终为紫红色,OD530nm值变化不大,说明氧化剂和还原剂对葵花壳红色素的稳定性影响较小。
2.2.5食品添加剂对葵花壳红色素稳定性的影响
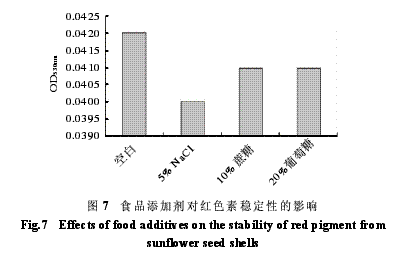
由图7可以看出:当向葵花壳红色素中加入食品添加剂,如NaCl、蔗糖、葡萄糖等,颜色均未发生变化,OD值变化不大,即以上食品添加剂对红色素的影响不大。
2.3葵花壳红色素初步纯化
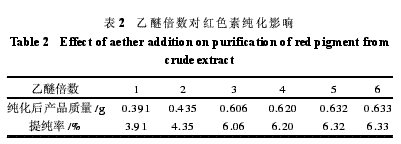
2.3.1加入乙醚倍数的影响
由表2可得,加入乙醚的倍数对红色素的纯化有一定影响,但红色素纯化时加入乙醚5~6倍所得的纯化色素几乎相等,而3~5倍略微相等,这可能是随着加入乙醚的倍数的增加,某些未来得及与红色素发生反应的乙醚与空气中的氧气生成过氧化乙醚造成乙醚的损失,也有可能所加入的盐酸-甲醇混合溶液,未完全溶解红色素粗提物,使得加入乙醚倍数3~5倍略微相等,考虑到成本,本实验在纯化过程中可加入乙醚3~5倍,本实验在纯化过程中可加入乙醚3~5倍。
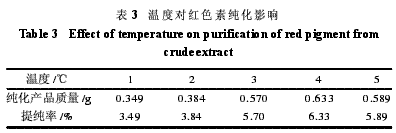
2.3.2置于冰箱中温度的影响置于冰箱中的温度对红色素的最终纯化结果有一定影响,由表3分析可得,4℃时纯化率相对较高,5℃提纯率低于4℃,这可能是高于5℃沉淀不完全造成红色素的损失,故选取4℃作为红色素浓浆静止于冰箱中的温度。
2.3.3扩大试验结果
称取20.0g葵花壳红色素粗品,按照1.4.2节对色素粗品进行纯化,得深紫红色粉末状固体色素1.26g,通过计算得葵花壳红色素提纯率为6.30%。
3·结论
3.1根据正交试验可以得出:影响葵花壳红色素提取的因素次序为超声温度>料液比>超声时间,葵花壳红色素的最佳提取条件为超声温度55℃、料液比1:16(g/mL)、提取时间10min;根据以上条件提取20.0g葵花壳并将葵花壳粗提后过滤的提取液浓缩至浓浆(呈膏状),纯化所得色素为深紫红色粉末状固体色素,提纯率为6.30%。
3.2据稳定性试验分析,温度、光照、p H值、金属离子、氧化剂、还原剂、食品添加剂对红色素的稳定性也会产生不同程度的影响。其影响结果如下:当温度≤80℃时,葵花壳红色素的稳定性较好;在一定光照条件下,光照时间越长,OD值越低,葵花壳红色素就越不稳定;pH值在1.0~2.0范围内,葵花壳红色素稳定性较好;在同一金属离子不同浓度的条件下,OD值变化不大,说明金属离子对葵花壳红色素稳定性的影响较小;不同浓度的氧化剂和还原剂的条件下,OD值变化均不大,说明氧化剂和还原剂对葵花壳红色素的稳定性影响较小;不同种类的食品添加剂对红色素的影响也较小。