流动注射分析在食品亚硝酸盐测定中的应用现状及发展趋势
流动注射分析(flow injection analysis,FIA)是1974年丹麦化学家Ruzicka和Hansen提出的一种新型的连续流动分析技术[1],是在封闭的管路中,在热力学非平衡条件下,向连续流动的载流断续地注入一定体积的样品,试剂与样品在混合圈中反应,然后流过检测器,由记录仪记录其吸光度、电位或者其他物理参数,一般输出峰形信号且峰高或峰面积与被测物浓度呈一次或二次相关,可利用峰面积或峰高对被测物进行定量分析(图1)。它是近20 年来才出现的一项分析技术,与其他分析技术相结合极大地推动了自动化分析和仪器的发展,成为一门新型的微量、高速和自动化的分析技术。特点是快速,不要求必须达到化学平衡,只要状态稳定就可以。
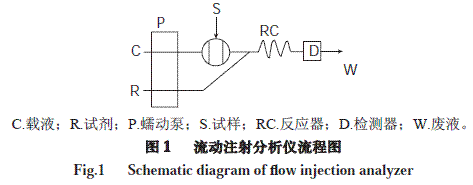
亚硝酸盐是一种毒性物质,俗称“工业用盐”,是一类无机化合物的总称,其外观及滋味都与食盐相似,人体长期摄入过量的亚硝酸盐可能引起血红蛋白变性和消化道癌变甚至可导致人体中毒死亡。联合国粮农组织和世界卫生组织规定[2],人体每天最多摄入亚硝酸钾或亚硝酸钠的量为0.2 mg/kg体质量。一次性大量摄入亚硝酸盐,会出现恶心、头晕、皮肤呈蓝褐、蓝灰或蓝黑色,一般以口唇、指端最为明显、全身无力、嗜睡,严重者呼吸困难、昏迷、抽搐,一般在食后0.5 h内发生,如不及时抢救,可在2 h内死亡[3]。
根据GB2760—2011《食品安全国家标准 食品添加剂使用标准》[4],亚硝酸钠和亚硝酸钾主要用于护色剂和防腐剂。根据规定可以用于腌腊肉制品,如咸肉、腊肉、板鸭、中式火腿、腊肠;酱卤肉制品类;熏、烧、烤肉类;油炸肉类;西式火腿类,如熏烤、烟熏、蒸煮火腿等;肉灌肠类;发酵肉制品类;肉罐头类等八类肉制品中,其最大使用量为0.15 g/kg。具体残留量除西式火腿为70 mg/kg、肉罐头类为50 mg/kg外,其他均为30 mg/kg。建立灵敏、快速、高效的食品中亚硝酸盐的检测方法尤为重要。当前我国食品中亚硝酸盐与硝酸盐的标准分析方法有盐酸萘乙二胺分光光度法和离子色谱法[5]。由于这些方法使用的有机试剂毒性较大,而且时间耗费比较长,近年来越来越多研究人员将流动注射技术运用在食品中亚硝酸盐的测定当中,以减小有毒试剂用量,避免过多的人手接触,实现简便、环保、快速大批量检测[6]。
本文综述了近年来国内流动注射分析在食品亚硝酸盐检测中的应用现状,对各种联用方法的原理、测定参数及其使用范围等进行了归纳总结,分析比较了各种方法的优劣,并对该领域的发展进行了展望,以期对我国流动注射技术测定食品中亚硝酸盐的发展提供一定的参考。
1· 流动注射分析测定食品中的亚硝酸盐
1.1 流动注射分光光度法
流动注射分光光度法一般是基于重氮化-偶联反应,即亚硝酸盐先与对氨基苯磺酸等发生重氮反应,再与偶联试剂(盐酸萘乙二胺、α-萘胺、N-(1-萘基)乙二胺、N-(1-萘基)乙烯二胺盐等)发生偶合反应,形成有色染料,其颜色深浅与亚硝酸盐含量成正比关系,从而可以用紫外-可见分光光度计来检测其中的亚硝酸盐含量[7-8]。流动注射分光光度法目前主要用于检测蔬菜类、肉类及水质中的亚硝酸盐含量。
任乃林等[9]将蔬菜匀浆后以超声波提取、活性炭脱色后,结合流动注射技术,建立流动注射分光光度法测定蔬菜中的亚硝酸盐含量。将样品中的亚硝酸盐与0.4%对氨基苯磺酸重氮化,再与0.2% N-(1-萘基)乙二胺盐酸盐偶合,在流动注射分析装置中,混合液在管路中停留300 s,接近完全反应,形成玫瑰色的偶氮染料,在540 nm波长处测定吸光度,可直接得到亚硝酸盐的含量。该亚硝酸盐检测方法的线性范围为0.1~2.4 μg/mL,检出限为0.01 μg/mL,相对标准偏差介于0.03%~1.8%之间,样品测定频率为10 个样/h。该方法精密度和准确度都很高,操作步骤比较简单、稳定,适用于不同亚硝酸盐含量蔬菜样品的测定。吴金苗等[10]应用流动注射法实现快速现场监测水中的亚硝酸盐含量,线性范围为0~60 μg/L,相对标准偏差为4%。将磺胺和盐酸萘乙二胺配成显色剂,结合流动注射分析仪,并用推动液(3%氯化铵)推动样品与显色剂混合,经过反应盘管生产红色偶氮染料,在535 nm波长处测定吸光度,从而达到快速监测水中的亚硝酸盐含量。该方法精密度好,大大降低了仪器装置的繁杂性,节省试剂,预先将磺胺与盐酸萘乙二胺配成显色剂,使操作更加简便,有利于在线分析。
Brabcova等[11]基于亚硝酸盐和盐酸介质中的利凡诺反应,利用流动注射分光光度法测定环境样品中的亚硝酸盐。得到的重氮盐在520 nm波长处测定吸光度。该方法亚硝酸盐的检出限为0.14 mg/L。而Chen Hui等[12]则基于亚硝酸盐和硫酸介质中的N-苯基邻氨基苯甲酸反应得到有色物质,利用流动注射分光光度法在410 nm波长处测定吸光度,检出限为2.5 ng/mL。Guerrero等[13]则利用硝酸盐和原黄素的反应通过流动注射分光光度法来进行检测。
1.2 流动注射催化(褪色)光度法
催化(褪色)光度法是在普通光度法的基础上发展起来的高灵敏度光度法,具有灵敏度高、检出限低等特点。一般是指基于在某种介质中,亚硝酸根离子催化某种氧化还原褪色反应(所用氧化剂主要有溴酸钾、氯酸钾、溶解氧、过硼酸钠和过氧化氢等;所用指示剂主要为偶氮染料、三苯甲烷类染料、对氮蒽染料及蒽醌类染料等),褪色程度与亚硝酸盐含量成正比关系,从而可以用紫外-可见分光光度计来检测其中的亚硝酸盐含量[14-17]。
张责珠等[18]利用在磷酸介质中,亚硝酸盐能催化溴酸钾氧化罗丹明B褪色反应的原理,建立了停留式流动注射催化光度法,该方法是以1.1 mol/L的磷酸溶液与4.0×10-5 mol/L罗丹明B混合为一路进样,样品溶液和8.5×10-2 mol/L的溴酸钾溶液分别为二、三路进样,在30 ℃的反应管中停留50 s,于555 nm波长处测定其吸光度。该法适用于水中痕量亚硝酸盐的测定,检出限为2.4×10-10 g/mL,具有高灵敏度,高选择性,简单快速的特点。
黄志勇等[19]利用硫酸介质中亚硝酸根催化溴酸钾氧化结晶紫褪色反应建立了反向停留流动注射光度分析法。首先将硫酸(0.1 mol/L)与溴酸钾溶液(0.08 mol/L)混合,再与结晶紫及样品混合后推入反应盘管停留30 s,在600 nm波长处测定吸光度。检出限为0.75 μg/L,在0.01~0.1 μg/mL范围内呈线性关系,可达到准确、可靠、快速测定饮用水及其他食品中的微量亚硝酸盐含量。而 Zhang Zhiqi等[20]在磷酸介质中进行了类似研究。
袁东等[21]利用一氯乙酸缓冲溶液中亚硝酸根对溴酸钾氧化亮绿具有催化的作用建立了流动注射催化光度法。预先将pH 2.7的一氯乙酸缓冲溶液与1.12×10-3 mol/L的亮绿溶液按3∶2的体积比混合8 h以上,再用流动注射仪控制溴酸钾(0.15 mol/L)和混合液流量为0.8 mL/min,试样和载流流量为1.5 mL/min,在室温下经过100 cm(内径为0.5 mm)的反应圈进行充分地反应混合,在624 nm波长处测定吸光度。检出限为7.44×10-4 mg/L,线性范围为0.04~0.36 mg/L,测定频率为60 次/h,相对标准偏差为1.1%。该方法要该方法适合测定自来水中的痕量亚硝酸盐含量。
龚正君等[22]利用亚硝酸盐对氯酸钠与亚甲基蓝发生的褪色反应有催化作用从而建立流动注射光度法。该方法在磷酸(0.80 mol/L)和硫酸(0.06 mol/L)混合介质中,结合流动注射技术,将样品、亚甲基蓝(50 μmol/L)和氯酸钠(0.2 mol/L)于80 ℃条件下充分混合反应后在670 nm波长处测定。检出限为1 μg/L,线性范围为质量浓度5~150 μg/L和150~1 000 μg/L。该方法与国家标准的光度法比,有反应灵敏、试剂环保、操作简单、自动化等优点。
1.3 流动注射化学发光法
化学发光法是具有灵敏、快速、操作简单、重现性好、可在线分析等优点而发展起来的一种方法,但是其选择性一般较差,所以排除干扰是完善化学发光法的一个重要方面。该方法一般先将亚硝酸根转化为一氧化氮,在气相中测定一氧化氮与臭氧反应的化学发光,但是这种方法仪器成本较高[23]。后来慢慢发展为基于亚硝酸根在特定pH值介质中能加强或减弱化学发光体系的化学发光偶合反应,用微光检测仪就可以完成检测。从而间接测定了亚硝酸盐的含量[24]。化学发光法主要使用反应体系为鲁米诺、罗丹明6-G、酸性铬蓝K等[25-26]。
龚正君等[27]利用亚硝酸根在酸性条件下与过氧化氢反应,其产物与碱性鲁米诺反应产生化学发光,从而建立了流动注射化学发光法检测水中的亚硝酸盐含量。使用0.1 mol/L硫酸作为体系中的催化剂,用0.3 mol/L氢氧化钠为1×10-8 mol/L的鲁米诺提供碱性条件,并使用100 μg/mL过氧化氢溶液与之发生化学发光反应。利用流动注射分析仪以2 mL/min的流速进样,测定反应的化学发光强度,从而计算出亚硝酸盐的含量。该方法检出限为1.6×10-3 μg/mL,线性范围是3.3×10-3~3.3 μg/mL,仪器设备简单,灵敏度高,线性范围宽,而且避免二次污染的优点,对水中亚硝酸盐在线检测提供了一种可靠的而简便的方法。Yaqoob等[28]也采用类似方法对新鲜水中的亚硝酸盐进行了测定。
肖新峰等[29]利用在酸性介质中,碘离子与亚硝酸根快速反应产生碘,碘氧化鲁米诺产生化学发光,并结合流动注射技术建立流动注射化学发光测定痕量亚硝酸根的方法,从而实现对痕量亚硝酸根的快速检测。使用HCl浓度为0.04 mol/L、KI质量分数为0.7%、鲁米诺浓度为4.0×10-4 mol/L、混合反应管长度为2.5 m。鲁米诺从主泵进样,流速为10 r/min;其他溶液从副泵进样,流速为20 r/min。主副泵运行时间为17 s。采样速率为20 次/min。检出限为0.5 μg/L,线性范围为1.0~10.0 μg/L以及10.0~100.0 μg/L。本方法已对水样、茶叶、大蒜、西红柿等得亚硝酸盐含量进行测定,并取得理想的效果。
吴婉娥等[30]利用亚硝酸根对溴酸钾-酸性铬蓝K体系的化学发光有显著的增强作用而建立了检测亚硝酸盐的新方法。使用0.5 mol/L的硫酸作为酸性介质、0.1 mol/L溴酸钾作为氧化剂、1.0×10-4 mol/L酸性铬蓝 K作为发光剂,进样流速为2.5 mL/min,从进样阀到微光检测间的管长为40 cm。该方法的检出限为1.1×10-10 mol/L。线性范围为1.0×10-8~8.0×10-5 mol/L,适合用于对水样进行检测,除具有快速、简单、灵敏度高的特点外,选择性较鲁米诺发光体系偶合反应方法好,不易被干扰。
王书民等[31]利用亚硝酸盐对高锰酸钾-乙二醛化学发光体系的抑制作用,建立了亚硝酸盐的流动注射发光测定的方法。该方法与之前方法不同的是,亚硝酸盐在这个反应中的作用并不是增强而是减弱发光强度。使用高锰酸钾的浓度为1.0×10-3 mol/L、盐酸溶液的浓度为0.4 mol/L、乙二醛溶液的体积分数为6%。采用管长12 cm,从进样阀到检测器间的管长为10 cm,所有管道的流速控制在3 mL/min。检出限为1×10-9 mol/L,线性范围为1.0×10-8~1.0×10-3 mol/L。本方法已对肉制品中亚硝酸盐含量进行测定,并得到可观的结果,与盐酸萘乙二胺分光度法检测出的结果没有很大差异。
王学锋等[32]利用亚硝酸根对鲁米诺-溴酸钾体系的化学发光具有显著增强作用,结合流动注射技术,建立了一种简单、快速测定亚硝酸根的方法。该实验发现亚硝酸根与溴酸根的反应产物参与鲁米诺的化学发光反应得到的响应信号是最大的。实验使用流速为3.6 mL/min,管道内径为0.8 mm,采样环长度为15 cm,选择0.18 mol/L的氢氧化钠作为鲁米诺溶液(1.0×10-6 mol/L)的介质,选择0.05 mol/L的硫酸作为溴酸钾溶液(0.03 mol/L)的介质。经过流动注射反应管后进入波长为425 nm的荧光分光光度计进行检测。检出限为2.0×10-3 mol/L,线性范围为4.0×10-3~4.0 mg/L。该方法适用于茶叶和蔬菜中的亚硝酸盐含量的测定。
2· 结语
目前亚硝酸盐对于人类来说就是双刃剑,一方面它是一种公认的潜在致癌物,另一方面它能抑制肉毒梭状芽孢杆菌生长,目前还无更优的替代物。因此目前人类还离不开它,所以在食品工业中如何安全使用亚硝酸盐备受关注[33]。
流动注射具有操作简便、试剂试样用量少、分析速度快、精度高、可与不同类型的检测手段联用等优点,适合现代分析监测和大批量样品分析的要求,发展较快。这就开启了流动注射法检测食品中亚硝酸盐的新局面[9,34-39]。到目前为止,食品中亚硝酸盐含量的检测方法有很多,分光光度法、催化光度法、化学发光法、离子色谱法、荧光光度法、示波极谱法、核固红共振光散射法等[40-42]。但是与流动注射联用的方法目前只有分光光度法、催化光度法、化学发光法。而且也只是少部分研究成果与流动注射技术结合使用,还有很多研究成果没有进一步与流动注射结合使用,提高检测效率,减少试剂用量,实现环保型检测。流动注射与其他检测方法联用分析测定食品中的亚硝酸盐含量的研究有很多,这些方法有各自的优缺点,适合不同样品的检测,但是每一种方法都是借助流动注射这个技术而达到更快速、更高效、更自动化和大批量检测的效果。因此,流动注射和其他分析方法联用的检测技术将会成为食品中亚硝酸盐含量检测技术发展的一个方向;需要不断地研究优化流动注射和其他检测方法联用的实验条件、仪器条件,以寻找最有效、最好的方法来测定食品中的亚硝酸盐。