食品中汞元素测定快速前处理方法研究
汞是一种具有生理毒性的重金属[1],由于具有累积性和环境持久性[2],会对自然环境造成污染并通过食物链富集转化进入人体,对机体造成以神经毒性和肾脏毒性为主的多系统损害,是人类健康的潜在威胁。国家标准《食品中总汞及有机汞的测定》[3]中样品前处理为高压消解、微波消解和低温回流消化等方法,高压和微波消解需要较昂贵的仪器设备,使用成本高,回流消化试剂用量大,耗时长,操作繁琐,对人员要求高,都不太适合样品的简单快速处理。现运用超声辅助[4]和控温加热辅助HNO3-H2O2、HNO3-HClO4快速提取食品中的汞元素,通过与依据国家标准GB /T5009. 17—2003 中微波提取-原子荧光光谱分析法的测定结果进行提取效率的比较,选择合适的匹配体系,并对试剂的用量比例、提取过程的温度控制等关键影响因素进行条件优化,初步建立一种简单有效提取食品中汞元素的快速前处理方法。
1 ·仪器与试剂
1. 1 仪器
AFS-230a 原子荧光光度仪及汞空心阴极灯( 北京吉天仪器公司) ; SMART MARS240 /50 微波消解仪( 美国CEM 公司) ; EHD-24L 型石墨消解仪( 北京东方科创生物技术有限公司) ; KQ-500DV 型数控超声波清洗器( 昆山市超声仪器有限公司) ; 全部实验器皿均用20%硝酸溶液浸泡24 h 以上,用去离子水多次冲洗晾干备用。
1. 2 试剂
汞标准溶液100 μg /ml( 中国计量科学研究院) GBW ( E) 080124; HCl、HNO3、HClO4、H2O2( 35% w /w) 为优级纯,其他为分析纯; 实验用水为18. 2 MΩ. cm 纯水。标准参考物质扇贝GBW10024( GSB—15) 和柑橘叶GBW10020 ( GSB—11) ( 地球物理地球化学勘查研究所) 。
2 ·实验步骤
2. 1 样品制备
市售干菌和干海带使用不锈钢粉碎机粉碎待用。
2. 2 标准参考物质
准备标准参考物质扇贝
GBW10024( GSB—15 ) 和柑橘叶GBW10020 ( GSB—11) 置于烘箱60℃烘4 h 后待用。
2. 3 样品处理
准确称取约0. 5 g 样品于长颈玻璃试管中,加入5 ml HNO3-H2O2( 4∶ 1) 和数滴辛醇,振摇混匀置于超声仪中,调整功率最大为40 kHz,水浴温度控制为80℃,超声时间60 min; 同样取样品加入5 ml HNO3-HClO4( 4 ∶ 1) ,振摇混匀置于石墨消解仪中,120℃加热60 min,待所有反应结束冷却后用纯水转移定容至25 ml 待原子荧光仪测定; 标准参考物质同样处理,并做试剂空白对照; 同时依据国家标准GB /T5009. 17—2003 第一法原子荧光光谱分析法采用微波消解样品后待仪器测定。
2. 4 标准曲线配制
准确吸取使用浓度为100 μg /L的汞标准溶液0. 05、0. 10、0. 30、0. 50、0. 70、1. 00 ml 于10 ml 容量瓶中,用HCl 溶液( 1 + 9) 定容至刻度,混匀待测。总汞的曲线范围为0. 5 ~ 10 μg /L,回归方程相关系数要求> 0. 999。
2. 5 仪器工作条件
光电倍增管负高压260 V,灯电流20 mA,原子化器高度8 mm,载气( Ar2) 流量400 ml /min,屏蔽气流量800 ml /min,以峰面积为读数方式。载流为3. 0% HCl,还原剂为1. 0% NaBH4溶液( 含0. 5%NaOH) 。
2. 6 统计学方法
应用统计软件SPSS 17. 0 对结果进行配对样本t 检验分析。
3 ·结果
3. 1 微波消解测定结果
采用微波消解-原子荧光光谱分析法连续测定干菌和干海带样品各6 次,干海带和干菌总汞含量分别为( 0. 39 ± 0. 06) mg /kg 和( 0. 82± 0. 05) mg /kg。
3. 2 实验条件选择
所用仪器测定方法和条件均参考GB /T5009. 17—2003 食品中总汞及有机汞的测定第一法,因此仅针对前处理方法进行条件选择。
3. 2. 1 预实验: 预实验可以保证测定过程的可行性和结果的准确性[5],实验发现超声辅助HNO3-HClO4提取的样液于仪器测定时与还原剂( 1. 0% NaBH4溶液)反应剧烈无法采集稳定信号; 控温加热辅助HNO3-H2O2的测定结果较另两种测定结果偏低,原因可能是H2O2在加热条件下温度越高自身的歧化反应越快,其氧化能力降低越快; 超声的水浴温度最高为100℃,相比石墨消解仪的加热温度较低,故HNO3-H2O2体系使用超声辅助提取,其样液与控温加热辅助HNO3-HClO4体系的样液均可用于原子荧光仪测定且具有良好荧光信号。
3. 2. 2 超声辅助HNO3-H2O2提取条件优化结果: 样品加入不同比例HNO3-H2O2后在不同温度条件下经超声辅助提取后的总汞测定结果,与微波消解测定结果相比计算提取效率,数据表明HNO3-H2O2比例4∶ 1,水浴温度80℃,提取60 min 后样品中汞元素的提取效率达到87%,为最佳提取条件( 表1) 。
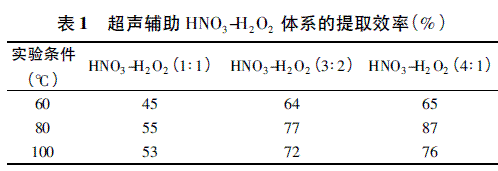
3. 2. 3 控温加热辅助HNO3-HClO4提取条件优化结果: 样品加入不同比例HNO3-HClO4后在不同温度条件下经加热辅助提取后的总汞测定结果,与微波消解测定结果相比计算提取效率,数据表明HNO3-HClO4比例4∶ 1,加热温度120℃ 时,提取60 min 后样品中汞元素的提取效率达到91% ,为最佳提取条件( 表2) 。
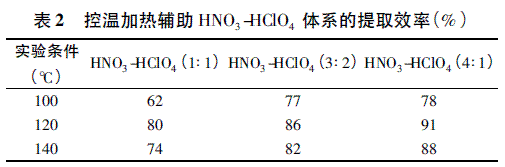
3. 3 样品测定结果及精密度实验
使用上述2 种最佳提取条件分别对干菌和干海带样品进行处理后测定,结果均值及相对标准偏差( RSD%) 见表3 和4。
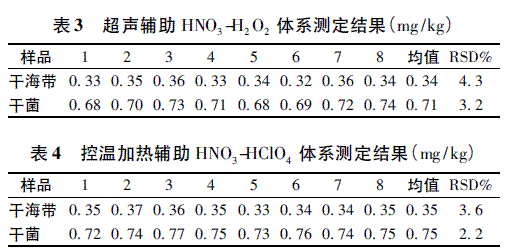
3. 4 准确度实验
分别按2 种最佳提取条件对标准物质扇贝和柑橘叶连续测定6 次,测定结果均在标准值要求范围之内( 表5) 。

3. 5 加标回收实验
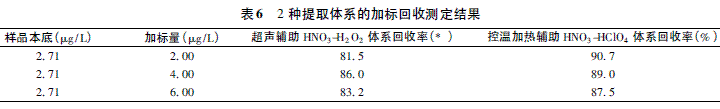
取一份干海带样品分别加入浓度为2. 00、4. 00 和6. 00 g /L 的汞标准溶液,再分别用2 种最佳提取条件测定加标回收率( 表6) 。
3. 6 超声功率的选择
超声波波长短频率高,穿透力强,具有冲击破碎和搅拌作用,已经应用到多种物质在多种介质的提取。在食品介质中提取汞元素,显著影响因素[6]为试剂比例,超声温度和超声时间,所以超声功率选择为最大40 kHz。3. 7 辛醇的作用辛醇作为消泡剂[7]可以有效抑制HNO3-H2O2体系中加入H2O2瞬间因氧化反应过于剧烈样品喷涌损失的现象,试剂空白对照实验表明辛醇对荧光测定无影响。
3. 8 消解管的选择
由于H2O2在加热条件下温度越高自身的歧化反应越快,即使加入数滴辛醇反应仍较剧烈,长颈试管延伸了反应空间,避免损失; 另外由于汞的易挥发性,选用细口长颈玻璃试管可以起到冷凝回流作用,进一步减少样品处理过程中汞的损失。
3. 9 结果分析
对于汞含量较低的干海带样品2 种测定结果差异无统计学意义( P > 0. 05) ,对于较高含量的干菌样品2 种测定结果差异有统计学意义( P < 0. 01) ,控温加热辅助HNO3-HClO4体系测定结果明显高于超声辅助HNO3-H2O2体系,原因可能是由于HClO4的氧化性高于H2O2,在开放式加热条件下对有机质的提取能力更强,对汞元素的提取会更完全; 实验表明控温加热辅助HNO3-HClO4体系在样品提取效率和精密度方面略优于超声辅助HNO3-H2O2体系; 2种提取方法的样品回收率在81. 5% ~ 90. 7% 之间,其中控温加热HNO3-HClO4辅助体系的加标回收率略高于超声辅助HNO3-H2O2体系,都符合《实验室质量控制规范食品理化检测》( GB /T27404-2008) [8]的要求。
4· 结论
实验数据和方法学参数表明,采用超声( 功率40 kHz水浴80℃) 辅助HNO3-H2O2( 4∶ 1) 和控温加热( 120℃) 辅助HNO3-HClO4( 4 ∶ 1 ) 这2 种方法快速( 60 min) 处理干海带和干菌样品,测定结果满意,两者都可作为简单快速有效提取食品中汞元素的前处理方法。